CRISPR: algas e moluscos possuem sistema similar
Sistema de edição genética presente em moluscos e algas, e similar ao CRISPR, pode ser chave para tratamentos em organismos complexos
Ronaldo Gogoni 41 semanas atrás
O CRISPR é hoje nossa melhor ferramenta para tratamentos de inúmeras doenças genéticas, detectadas na fase embrionária, e até algumas em organismos já formados. A técnica de edição genética é aplicável também no combate a outras enfermidades, no que vem há muito tempo sendo estudada para tratar a AIDS.
- CRISPR - Entenda o que é e quais as possibilidades, sem hype ou histeria
- CRISPR contra o HIV, agora com menos polêmica
Claro, em Biologia nada é 100% exato, o método usado hoje possui limitações, uma das principais ser mais difícil empregar a edição em organismos complexos. Exatamente por isso, muitos estão eufóricos com a descoberta de que vários espécimes, de moluscos a algas, possuem um sistema de edição similar ao CRISPR, que pode ser até mais simples de usar por pesquisadores e médicos.
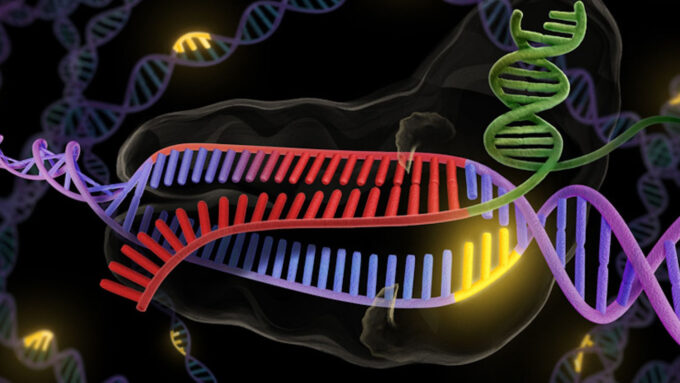
O CRISPR usa a enzina Cas9 copiada de bactérias; o método funciona, mas cria alguns problemas (Crédito: Jennifer A. Doudna/UC Berkeley)
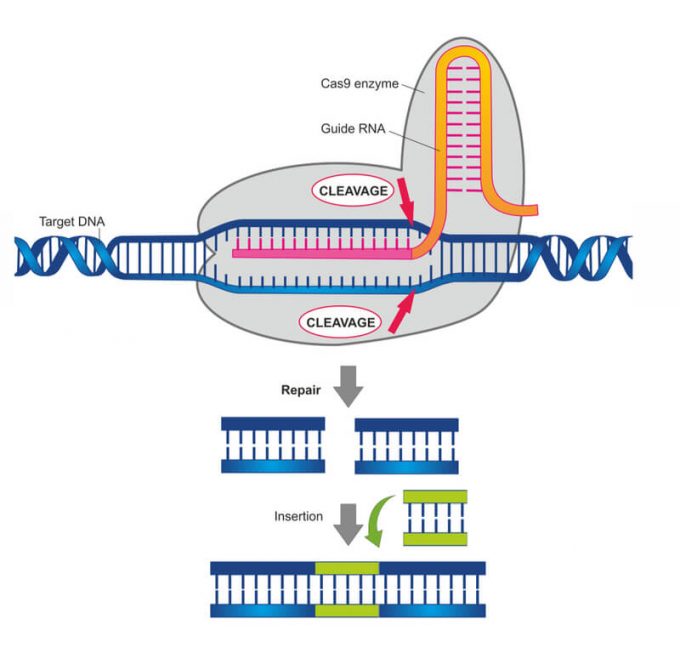
Como já explicamos hoje, o CRISPR funciona como um mecanismo de defesa de bactérias e arqueias, que são organismos procariontes, isto é, unicelulares desprovidos de núcleo e organelas; diferente de células eucariontes, que compõem organismos complexos, o material genético destas está "solto" em seu interior.
Por serem muito simples, esses seres são alvos constantes de vírus, mas a Evolução lhes permitiu contar com defesas. Quando um DNA invasor adentra a célula, esta ativa uma série de proteínas chamadas Cas1, que copiam um trecho do código genético e o repassam para ua enzina, chamada Cas9. Quando esta identifica uma sequência igual, ativa uma "tesoura" que corta, fisicamente, o gene naquele exato ponto, o inutilizando.
O método completo de edição genética do CRISPR foi desvendado pelos professores Francisco Mojica e Ruud Jansen, e em 2012, as Dras. Jennifer A. Doudna e Emmanuelle Charpentier desenvolveram um método que usa a tesoura do Cas9 com sequências de DNA editados pela mão humana, para desligar genes e cromossomos específicos, representando um avanço gigante no combate a doenças como anemia falciforme, fibrose cística e esclerose múltipla, e até corrigir, em fase embrionária, síndromes como Down, Turner e Patau, anomalias causadas por cromossomos X e/ou Y extra, e por aí vai.
O desenvolvimento do CRISPR como técnica de tratamento rendeu a Doudna e Charpentier o Prêmio Nobel de Química de 2020, algo mais do que merecido.
O CRISPR permite uma série de possibilidades, e até tratar doenças com organismos já formados, mas ele funciona melhor com células mais simples, sendo mais empregado em pesquisas que envolvem gametas ou embriões em estágios iniciais. Para o tratamento de doenças, há outro fator de complicação, pois o método de injeção da enzima Cas9 geralmente usa vírus, com moléculas copiadas de bactérias como Staphylococcus aureus e Streptococcus pyogenes.
Ambas são causadoras de doenças e infecções, que vão de meningite e faringite a condições realmente graves, como síndrome do choque tóxico, sepse, e escarlatina. Desnecessário dizer que o corpo humano ODEIA esses caras, e quando detecta traços deles, aciona um exército de linfócitos T, programados para Buscar e Destruir tudo o que identificam como células perigosas, incluindo as infectadas por patógenos.
Em um estudo publicado na Nature, foi detectado que 79% dos humanos possuem anticorpos contra a Cas9 desenvolvida com a S. aureus, e 65% deles contam com defesas que afetam a enzima produzida com base no S. pyogenes.
Ou seja, as células alteradas pelo CRISPR são eliminadas sumariamente, ao serem tratadas como ameaças ao organismo.

Os linfócitos T são adeptos da filosofia "destrua primeiro, pergunte depois", não por acaso, são chamadas em inglês de "killer T cells" (Crédito: Reprodução/David Production)
O outro grande problema do CRISPR é sua precisão. A "tesoura" da Cas9 é capaz de cortar o ponto exato que bate com a cópia do DNA que ela contém, mas não raro, ela pode cortar mais do que devia, eliminando porções maiores de uma sequêcia, que acaba se colando de qualquer jeito e repassando informações defeituosas.
Essa perda de material relevante, que pode chegar a até 10%, descamba muitas vezes em um processo descontrolado de replicação celular, ou seja, câncer. E é aqui que a pesquisa mais recente entra.
Fanzor é mais preciso que CRISPR
O estudo (cuidado, PDF) conduzido pelo prof. Feng Zhang, filiado ao Instituto McGovern para Pesquisa Cerebral e ao Instituto Broad, ambos do MIT (o segundo também com Harvard), visava investigar a origem da Cas9, no que foi identificado seu "ancestral", uma classe de proteínas chamadas OMEGA. Uma delas, chamada TnpB, possui similaridades com outra presente em organismos eucariontes, conhecida como Fanzor.
Levantou-se então a suspeita de que esta proteína poderia direcionar enzimas, como as Cas1 fazem com a CRISPR-Cas9, para acionar sua própria versão de "tesoura" genética. Para isso, os pesquisadores isolaram proteínas de algas, fungos, amebas, e da amêijoa-mercenária (Mercenaria mercenaria), uma espécie de berbigão, ou "vongole" comestível (o certo seria "vongola", o singular em italiano, mas enfim), para testar a hipótese, e o modelo bateu direitinho.
A endonuclease (enzima) Fanzor-ωRNA é guiada por partes do DNA das células desses organismos, e faz o mesmo que a CRISPR-Cas9. Elas estão presentes em transpósons, genes "saltadores" que se autorreplicam em um genoma, e por serem mais compactas, podem fazer cortes em sequências com mais precisão do que sua versão procarionte.

A amêijoa-mercenária (Mercenaria mercenaria) é um dos vários organismos complexos que usam o sistema Fanzor-ωRNA de edição genética (Crédito: Ken Hammond/U.S. Department of Agriculture/domínio público)
Em tese, a Fanzor-ωRNA teria maior compatibilidade com o organismo humano, por ser produzida no mesmo tipo de células eucariontes que possuímos; por outro lado, ainda não está claro seu papel natural em organismos multicelulares complexos, já que com exceção do molusco, todos os outros organismos que foram alvos da pesquisa são unicelulares, como as bactérias e arqueias que possuem o Cas9.
As implicações
Por ser menor que a CRISPR-Cas9, a enzima Fanzor-ωRNA seria capaz de realizar incisões em DNAs-alvo com uma menor margem de erro, reduzindo em muito o risco de mutações genéticas e aumento nas chances de um paciente desenvolver câncer.
Além disso, a enzima pode ser alterada in vitro para aumentar sua eficiência, o que foi feito com amostras retiradas de fungos, que originalmente não apresentavam os mesmos resultados da Cas9. Por fim, as chances de que a inserção dessas células no corpo humano não disparem o alarme dos linfócitos T, ao menos, não no mesmo grau do notado com a enzima tirada de bactérias.
Claro, ainda é bastante cedo para dizer que este método vai resolver os problemas do método de CRISPR que usa a Cas9, e ainda deverá levar muito tempo até desenvolvermos um método eficaz de uso da Fanzor-ωRNA em tratamentos e pesquisas, mas é um sinal de que o sistema das bactérias não é único na Natureza, e podem existir outros, ainda mais eficientes, esperando para serem descobertos.
Talvez, um novo sistema possa permitir níveis de edição genética que nem a Cas9 ou a Fanzor-ωRNA serão capazes de viabilizar.
Só não se empolgue muito, dificilmente chegaríamos a algo como catgirls.
Referências bibliográficas
SAITO, M., XU, P., FAURE, G. et al. Fanzor is a eukaryotic programmable RNA-guided endonuclease. Nature (2023), 50 páginas, 28 de junho de 2023. Disponível aqui.
Fonte: ExtremeTech